
1. Zielsetzung
Ziel dieses Versuchs ist es, die chemisch-physikalische Wirkung von Gallium (Ga) auf Aluminium (Al) zu untersuchen. Dabei soll gezeigt werden, wie das Auftragen von flüssigem Gallium die mechanische Festigkeit von Aluminium stark herabsetzt bis zur Zerstörung. Die Beobachtungen dienen dem Verständnis von metallischen Bindungen, Kristallstrukturen und deren Störungen durch Fremdatome.
2. Versuchsaufbau
Hinweis: Dieser Beitrag enthält Affiliate-Links. Wenn du über diese Links etwas kaufst, erhalte ich eine kleine Provision – für dich entstehen keine Mehrkosten.
Benötigtes Materialien:
- Ein kleiner Aluminium-Gegenstand (z. B. ein Stück Alufolie, ein Getränkedosen-Deckel oder ein Aluminiumstab)
- Eine geringe Menge Gallium (flüssig bei Raumtemperatur ab etwa 29,8 °C) – zum Produkt
- Ein Glas oder Kunststoffgefäß (kein Metall, da Gallium auch mit anderen Metallen reagieren kann)
- Schutzhandschuhe – zum Produkt
- Schutzbrille – zum Produkt
- Pipette oder kleiner Löffel (zum Dosieren des flüssigen Galliums) – zum Produkt

Durchführung:
Das Aluminiumstück wird gereinigt, um Oxidschichten und Fette zu entfernen (z. B. mit etwas Alkohol). Dann wird es leicht angekratz damit das Gallium in das Aluminium eindringen kann.
Eine kleine Menge flüssiges Gallium wird mit einer Pipette oder Holzstäbchen auf die Oberfläche des Aluminiums aufgetragen. Das Aluminiumstück wird einige Stunden bei Raumtemperatur liegen gelassen.
Danach kann man versuchen das Metall leicht zu verbiegen oder zu zerdrücken.
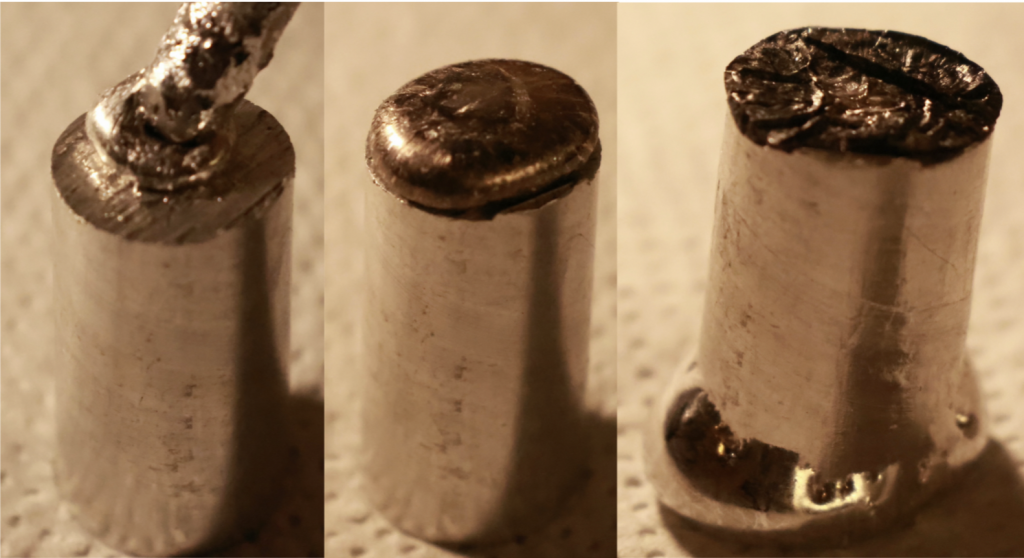

3. Ergebnisse
Bereits nach kurzer Zeit dringt das Gallium in das Aluminium ein. Das ursprünglich feste, silbrig-glänzende Metall verliert seine Stabilität und lässt sich leicht zerdrücken oder zerbröckeln.
Der Grund: Gallium diffundiert in das Kristallgitter des Aluminiums und unterbricht die metallischen Bindungen zwischen den Aluminiumatomen. Dadurch wird die für Metalle typische Bindung durch Elektronengas gestört. Außerdem verhindert Gallium die Bildung der normalerweise schützenden Oxidschicht (Al₂O₃), wodurch weitere Reaktionen stattfinden können.
Auf mikroskopischer Ebene entstehen intermetallische Phasen und kristalline Störungen, die zu einem spröden, körnigen Material führen. Aluminium verliert somit nahezu vollständig seine mechanische Festigkeit.
4. Schlussfolgerung
Der Versuch zeigt eindrucksvoll, wie empfindlich selbst stabile Metalle auf bestimmte Fremdelemente reagieren können. Gallium zerstört Aluminium nicht durch klassische chemische Korrosion, sondern durch interkristalline Diffusion und Bindungsstörung.
Dieses Phänomen hat praktische Bedeutung: In der Luft- und Raumfahrt oder im Maschinenbau muss der Kontakt von Gallium mit Aluminium unbedingt vermieden werden, da bereits kleine Mengen zu strukturellen Ausfällen führen können.
Für den Unterricht oder Demonstrationszwecke ist der Versuch gut geeignet, um das Verständnis für metallische Bindungen, Kristallgitterstrukturen und Materialzerstörung durch Diffusion zu fördern.
Er ist ungefährlich, leicht durchzuführen und liefert beeindruckende visuelle Ergebnisse.

Gallium ist wenig flüchtig und nicht hochgiftig, kann jedoch Haut und Kleidung verfärben.
Kontakt mit Aluminium vermeiden! Gallium kann Legierungen mit Aluminium bilden und das Material beschädigen.
Nicht in den Abfluss schütten! Gallium ist recycelbar – Reste in einer verschließbaren Schale sammeln und an eine geeignete Rücknahmestelle oder das Labor zurückgeben.
Sicherheitshinweise

Keine offene Flamme oder starke Hitze verwenden – das Wasserbad reicht zum Schmelzen aus.
Schutzbrille und Handschuhe tragen.
Bei Hautkontakt sofort mit Wasser und Seife abwaschen.
In gut belüfteter Umgebung arbeiten.


Schreibe einen Kommentar