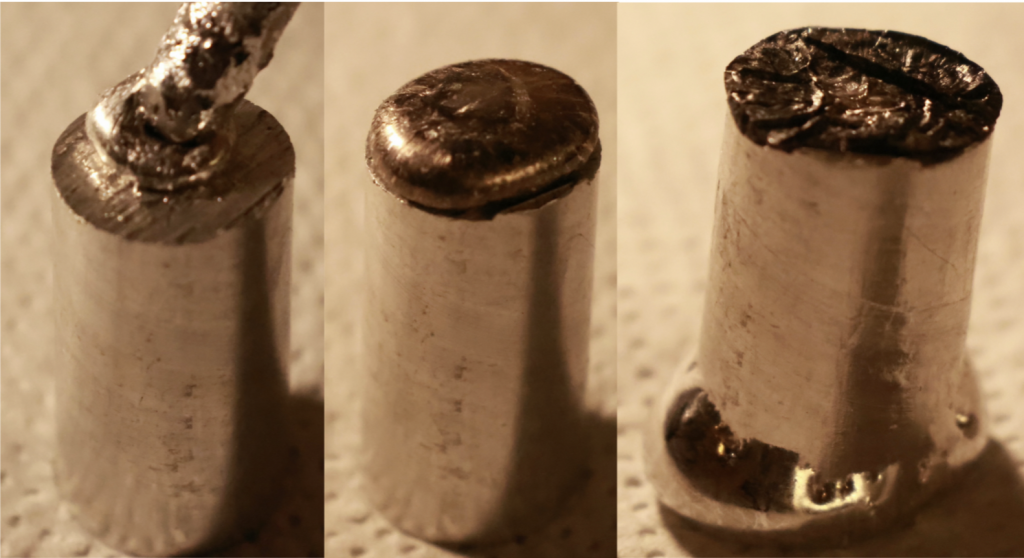1. Zielsetzung
Hier wollen wir den faszinierenden Lotoseffekt genauer unter die Lupe nehmen, jenes erstaunliche Naturphänomen, das dafür sorgt, dass Schmutz und Wasser auf den Blättern der Lotosblume einfach abperlen. Dazu brauchen wir nur Papier, Serviette, Lumpen und Gallium.
Unsere Aufgabe besteht darin herauszufinden, wie sich Gallium , ein außergewöhnliches Metall, das bei Körpertemperatur schmilzt – auf diesen verschiedenen Oberflächen verhält. Wird es an ihnen haften bleiben, oder perlt es wie ein Wassertropfen auf einem Lotosblatt ab?
2. Versuchsaufbau
Hinweis: Dieser Beitrag enthält Affiliate-Links. Wenn du über diese Links etwas kaufst, erhalte ich eine kleine Provision – für dich entstehen keine Mehrkosten.
Benötigtes Material:
- Gallium (Metall, fest bei Raumtemperatur) – zum Produkt
- Becher oder kleine Glasgefäße
- Warmes Wasserbad (zum Schmelzen des Galliums)
- Pipette oder kleiner Löffel (zum Dosieren des flüssigen Galliums) – zum Produkt
- Papier
- Stoff (Lumpen)
- Serviette
- Schutzhandschuhe – zum Produkt
- Schutzbrille – zum Produkt



3. Ergebnisse
Beim Kontakt mit dem Papier sowie der Serviette zeigte das Gallium eine deutlich hydrophobe Wechselwirkung. Es perlte auf der Oberfläche ab, ohne in das Material einzudringen oder eine sichtbare Benetzung zu zeigen. Dies weist darauf hin, dass die Oberflächenenergie dieser Materialien nicht ausreicht, um eine stabile Haftung oder Reaktion mit dem flüssigen Metall zu ermöglichen.
Im Gegensatz dazu verhielt sich das Gallium auf dem Stofftuch deutlich anders. Hier bildete sich keine Tropfenstruktur; stattdessen löste sich beim Kontakt eine dünne Schicht des Galliums ab, die sich mit den Fasern des Gewebes verband. Dieses Verhalten deutet auf eine mögliche mechanische oder chemische Wechselwirkung zwischen dem Gallium und den Bestandteilen des Stoffes hin, die eine teilweise Adhäsion oder Oberflächenreaktion zur Folge hatte.
4. Schlussfolgerung
Die Ergebnisse des Experiments verdeutlichen, dass das Benetzungsverhalten von flüssigem Gallium stark von den physikalischen und chemischen Eigenschaften der jeweiligen Oberfläche abhängt. Während Gallium auf Papier und Papierserviette aufgrund ihrer porösen, aber wenig reaktiven Struktur keine Haftung zeigt und als Tropfen abperlt, kommt es auf dem Stofftuch zu einer deutlicheren Wechselwirkung. Das Ablösen einer dünnen Galliumschicht weist darauf hin, dass bestimmte Materialien – insbesondere solche mit textiler oder faseriger Struktur – eine stärkere Adhäsion oder sogar eine oberflächliche Reaktion mit Gallium ermöglichen können.
Diese Beobachtungen lassen sich dahingehend interpretieren, dass Gallium empfindlich auf Unterschiede in Oberflächenenergie, Materialstruktur und chemischer Zusammensetzung reagiert. Für weiterführende Untersuchungen wäre es daher interessant, den Einfluss verschiedener Gewebetypen oder Oberflächenbehandlungen systematisch zu analysieren, um die Wechselwirkungen von Gallium mit organischen und anorganischen Materialien besser zu verstehen.

Gallium ist wenig flüchtig und nicht hochgiftig, kann jedoch Haut und Kleidung verfärben.
Kontakt mit Aluminium vermeiden! Gallium kann Legierungen mit Aluminium bilden und das Material beschädigen.
Nicht in den Abfluss schütten! Gallium ist recycelbar – Reste in einer verschließbaren Schale sammeln und an eine geeignete Rücknahmestelle oder das Labor zurückgeben.
Sicherheitshinweise

Keine offene Flamme oder starke Hitze verwenden – das Wasserbad reicht zum Schmelzen aus.
Schutzbrille und Handschuhe tragen.
Bei Hautkontakt sofort mit Wasser und Seife abwaschen.
In gut belüfteter Umgebung arbeiten.